Wirksame Strategien für Rettungsstudien
Verifizierung von Protokollannahmen
Validierung der Studienpopulationsgröße
Überprüfung der statistische Analysepläne
Validierung statistischer Berechnungen
Audits der Datenqualität
Seit 20 Jahren helfen wir unseren Partnern auf effektive Weise und mit den höchsten Qualitätsstandards klinische Projekte und Beobachtungsstudien durchzuführen.

Qualität und Sicherheit
Sicherstellung der Umsetzung von Projekten gemäß den geltenden Industriestandards (inklusive GCP und FDA CFR 21 Teil 11). Garantie für hohe Qualität und Datensicherheit, die sowohl durch die ISO 9001 und 27001 Zertifizierungen als auch eine Reihe von internen SOP Prozeduren bestätigt ist.
Volle Studienunterstützung
Professionelle Realisierung jeder Phase des Projekts in Zusammenarbeit mit einem interdisziplinären Team von Spezialisten, die Erfahrung in der Durchführung von internationaler Forschung haben.
Moderne Technologien
Verwendung von modernen und effektiven IT-Tools, die eine flexible Anpassung an die spezifischen Anforderungen jeder Studie ermöglichen. Freiheit zur Integration von externen Datenquellen, wie Mobilgeräte, moderne medizintechnische Geräte, Datenbanken für Medizinsysteme.
Neuigkeiten
CRO Dienstleistungen
2KMM CRO ist ein vertrauenswürdiger Anbieter umfassender Dienstleistungen und Lösungen, die das Management und die Durchführung von Forschungsprojekten in der Pharma-, Biotechnologie-, Medizinprodukte- und Gesundheitsbranche unterstützen.
Als CRO-Unternehmen (Contract Research Organization) bieten wir die professionelle Durchführung von Aufgaben in den folgenden Bereichen klinischer Studien:

GoResearch™.live
GoResearch™.live ist eine vollständig validierte, moderne EDC-Plattform (Electronic Data Capture - EDC) der nächsten Generation, entwickelt für klinische Studien und Beobachtungsstudien. Sie ermöglicht eine schnelle, codefreie Erstellung individuell anpassbarer elektronischer Case Report Forms (eCRFs), bietet eine robuste Echtzeit-Datenvalidierung und erfüllt vollständig die Anforderungen der FDA 21 CFR Part 11, GCP und DSGVO. Die Plattform wurde für maximale Flexibilität konzipiert und unterstützt alle Studienformate – von traditionellen über hybride bis hin zu dezentralen Studien. Die sichere API erlaubt eine nahtlose Integration externer Systeme und erweitert Studien um elektronische Quelldaten (eSource) sowie Real World Data (RWD). Mit intuitiven Tools und Echtzeit-Überwachung optimiert GoResearch™.live optimiert die Datenerfassung und Steigerung der Studieneffizienz.
mehr ...GoResearch™ App
GoResearch™ App ist eine dedizierte mobile Anwendung für Patienten oder Kliniker, die die Erfassung von Forschungsdaten mithilfe elektronischer Fragebögen (z. B. ePRO oder eCOA) oder verbundener mHealth-Geräte unterstützt. Die App ist vollständig in die eCRF-Plattform integriert und bietet eine sofortige Datenübertragung zur Forschungsdatenbank und direkte Kommunikation in Form von Warnungen und/oder Erinnerungen. Verfügbar für Android und iOS.
GoInsights™
GoInsights™ ist eine allgemeine Plattform, die die freie Erstellung von beliebegen Datenerfassungstools oder Präsentationen ermöglicht. Die Formen ePRO-, eCOA-, eIC- als auch die Leiter-Schulungsformen können mit verschiedenen Bearbeitungskomponenten erstellt und mit Multimedia-Inhalten angereichert werden. Die Plattform wurde für optimale Leistung und Komfort für Benutzer von Desktop-Computern und Mobilgeräten entwickelt. Es kann im Standalone-Modus ausgeführt oder in die GoResearch™ -Plattform integriert werden.
mehr ...
Projektmanagement
Vorbereitung und Management
der Studiendokumentation
Die Rekrutierung von Studienzentren
und Patienten
Überwachung der klinischer Prüfungen
Studienzentrenmanagement
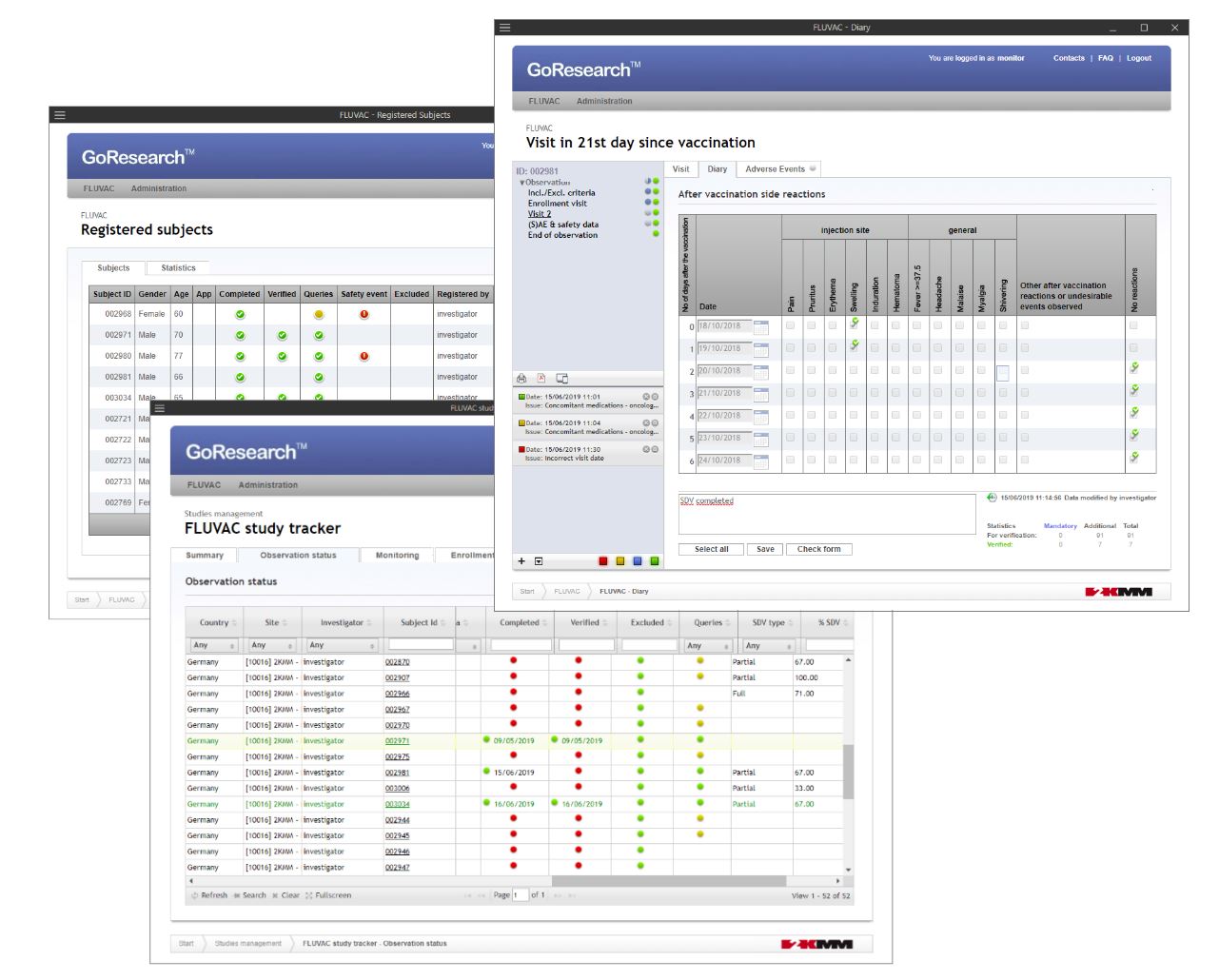
Gestaltung und Vorbereitung von eCRF's
Datenmanagementpläne
Datenvalidierungspläne
Nachfragemanagement (queries)
Medizindatenkodierung
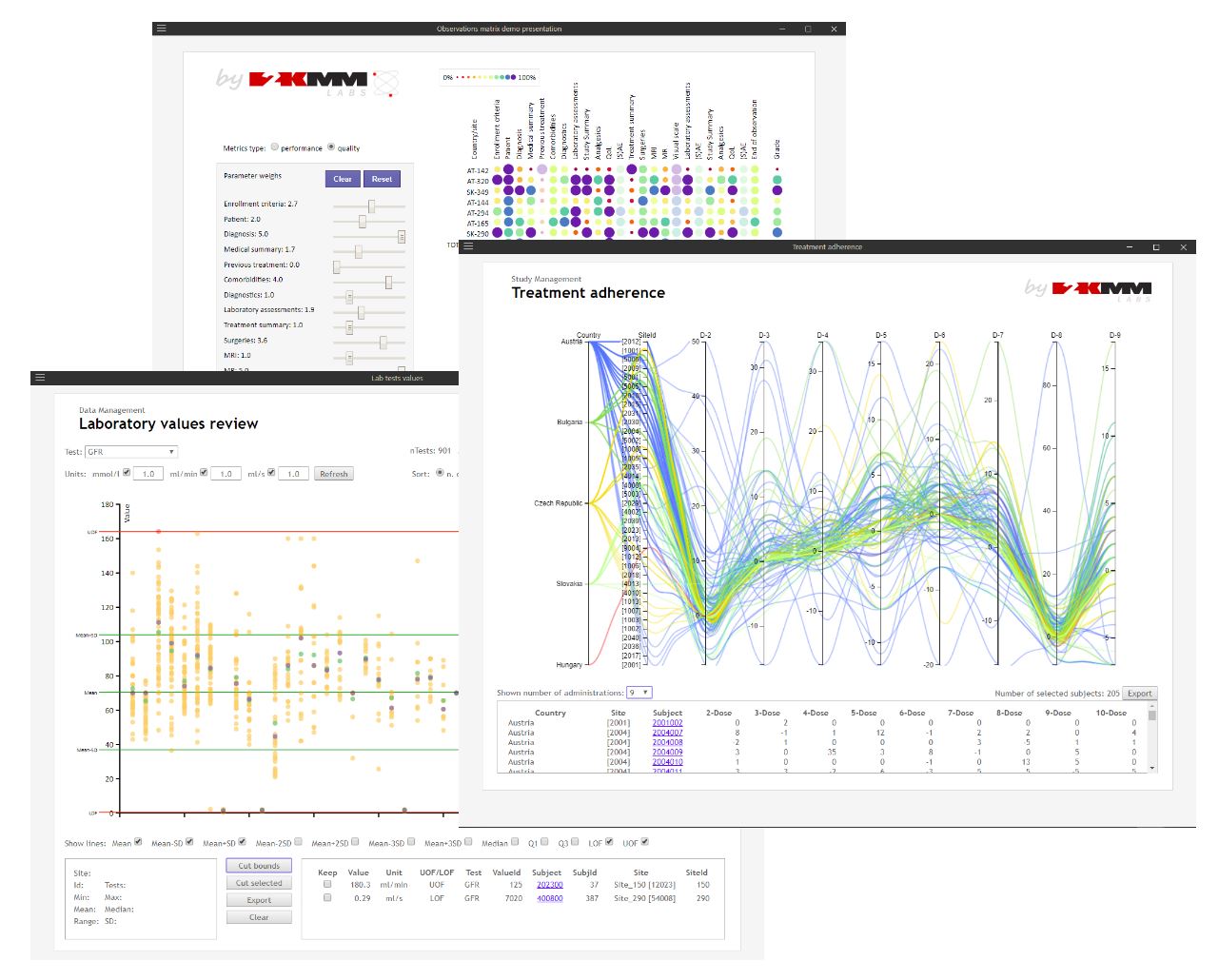
Unterstützung im Protokollschreiben
statistische Analysepläne
Design und statistische Analyse
Forschungsberichte
Randomisierung und Verblindung

Protokolle
Prüfarztbroschüren
Studienberichte (CSR)
Manuskripte
Abstracts

Überwachung unerwünschter Ereignisse
Sicherheitsdatenbankpflege
SAE/SUSAR/USADE-Berichterstattung
Sicherheitsmanagementpläne
Sicherheitsrichtlinien
Verfassen von Fallberichten
Periodische Berichte





